非臨床試験/臨床成績/主要文献
非臨床試験
(1)基質特異性(in vitro)9)
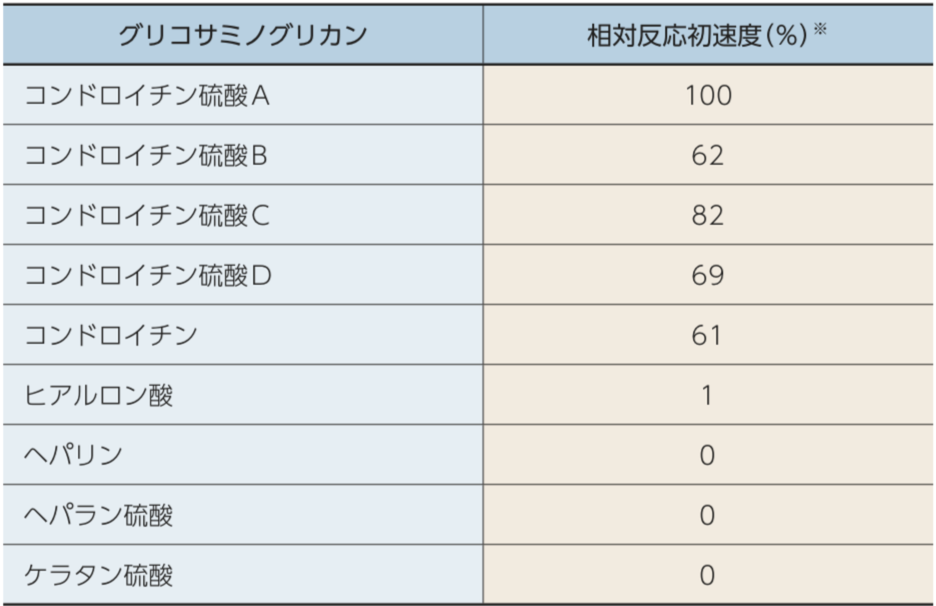
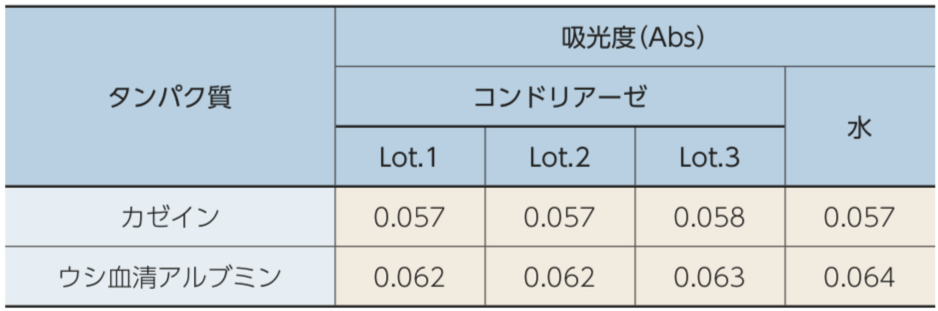
コンドリアーゼのグリコサミノグリカンに対する分解活性を各基質における反応初速度で求めたところ、コンドロイチン硫酸、コンドロイチン及びヒアルロン酸に対して分解活性を有し、ヘパリン、へパラン硫酸及びケラタン硫酸には作用しなかった。また、280nm吸光度測定を用いてコンドリアーゼのタンパク質に対する反応を評価したところ、コンドリアーゼを添加したカゼイン溶液及びウシ血清アルブミン溶液において吸光度上昇は認められず、タンパク質分解活性を有しないことが示された。
コンドリアーゼは、グリコサミノグリカンであるコンドロイチン硫酸、コンドロイチン及びヒアルロン酸を特異的に分解した。
コンドリアーゼの基質特異性(多糖類)
コンドリアーゼの基質特異性(タンパク質)
(2)椎間板高狭小化作用(ウサギ)10)
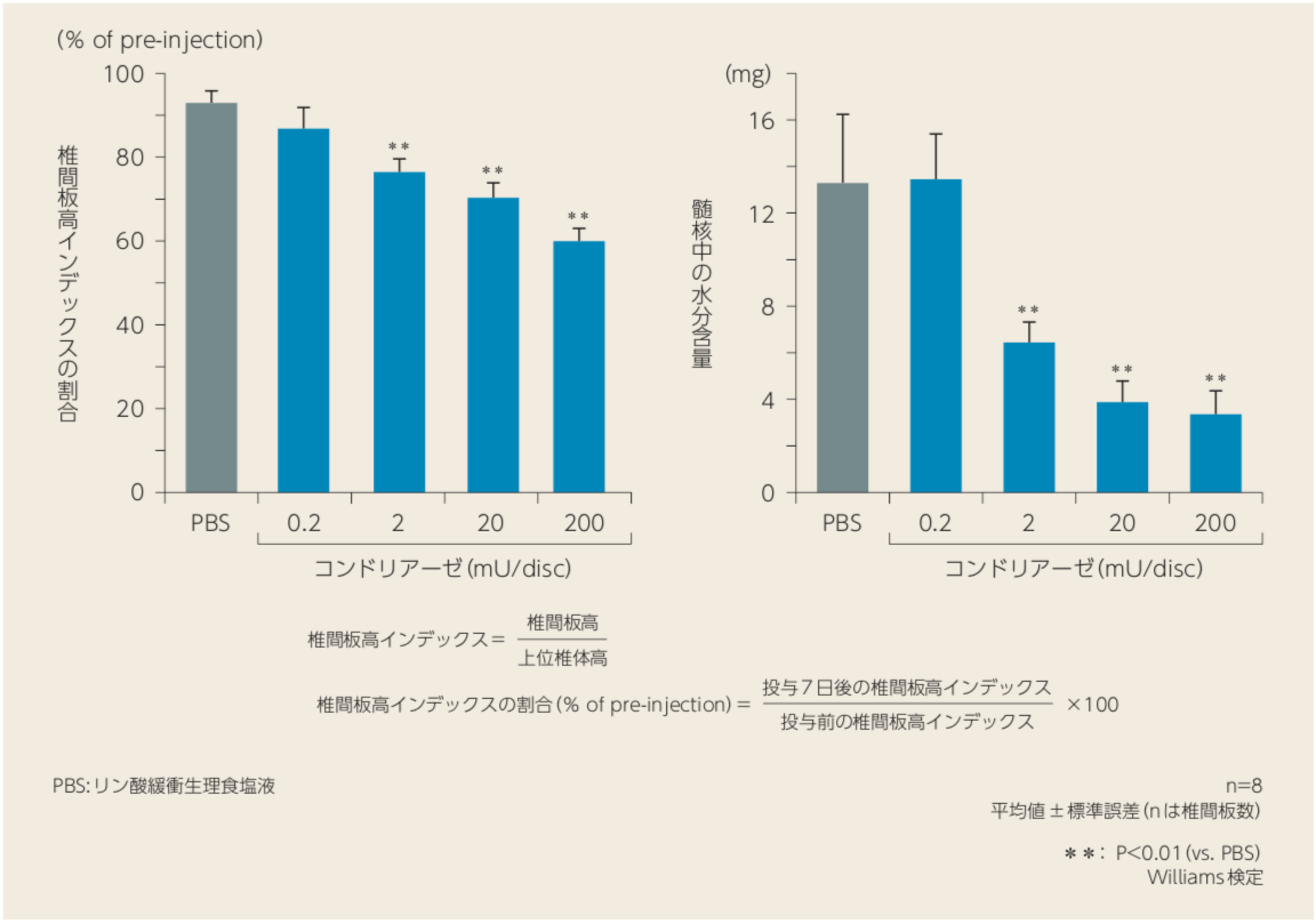
正常なウサギの椎間板内にコンドリアーゼを単回投与することにより、髄核の水分含量が減少し、椎間板高の狭小化が認められた。
ウサギにおけるコンドリアーゼの椎間板高及び髄核水分含量に対する作用
- 【方法】
- 正常なウサギ椎間板内に、コンドリアーゼを0.2、2、20又は200m単位(U)/discの用量で単回投与した。対照群にはPBSを単回投与した。投与前及び投与後7日にX線撮影を行い、投与前の椎間板高インデックスを100%とした際の投与後7日における椎間板高インデックスの割合を求めた。また、水分含量は投与後7日に髄核を摘出して測定した。
- 【結果】
- コンドリアーゼを単回投与することにより、用量依存的に椎間板高インデックスの割合を減少させた。コンドリアーゼ2、20及び200mU/disc 群ではPBS群と比較し椎間板高インデックスと髄核中の水分含量に有意差が認められた。また、これらコンドリアーゼによる椎間板高インデックスの割合の減少と髄核水分含量の減少には相関(r=0.765)が認められた。
10)より一部改変
(3)椎間板内圧低下作用(ヒツジ)11)
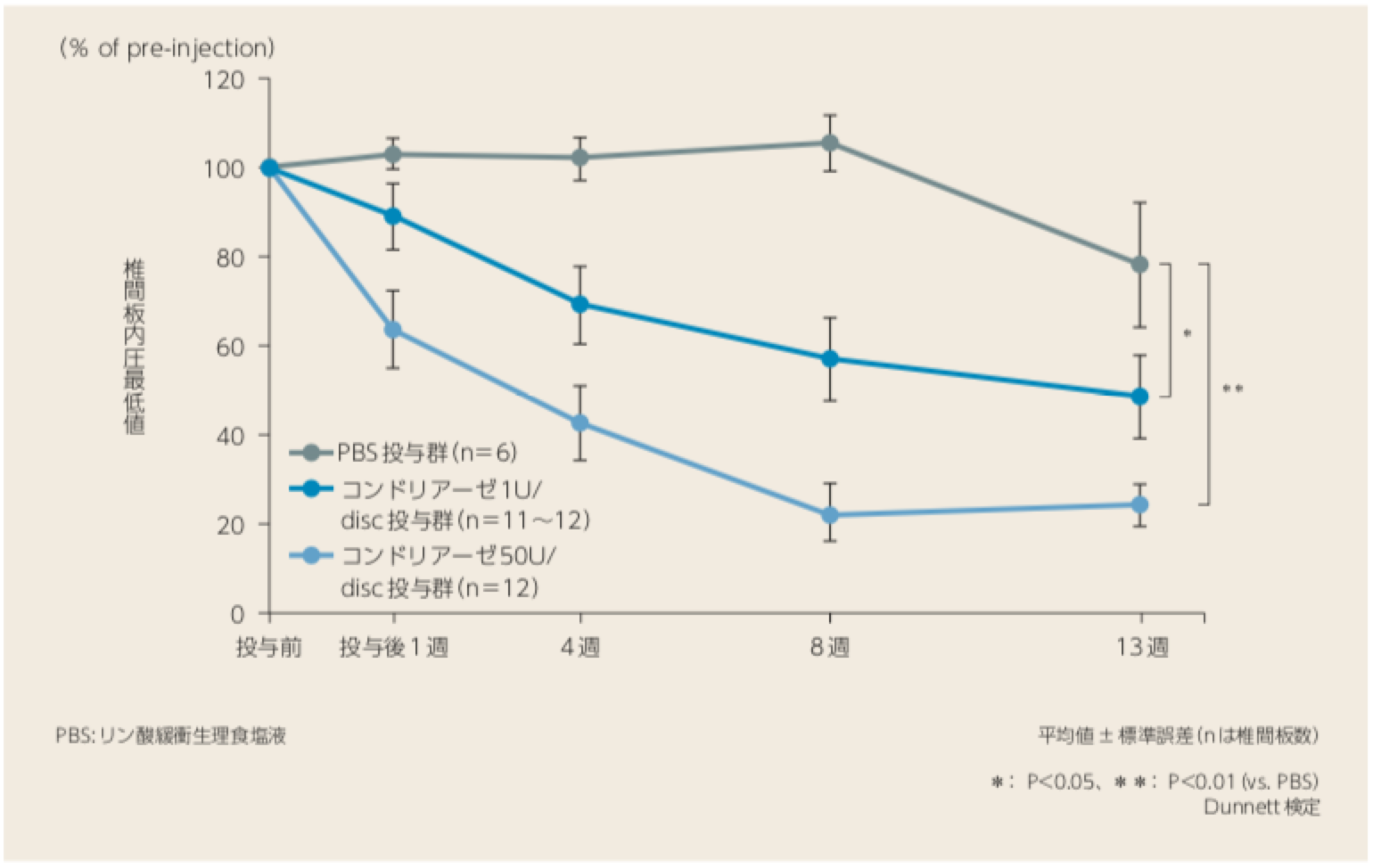
正常なヒツジの椎間板内にコンドリアーゼを単回投与することにより、椎間板内圧の低下が認められた。
ヒツジにおけるコンドリアーゼ投与後の椎間板内圧最低値の経時的推移
- 【方法】
- 正常なヒツジの椎間板内に、コンドリアーゼを1単位(U)/disc又は50U/discの用量で0.2mL単回投与した。対照群にはPBSを単回投与した。投与前2~7日、投与後1、4、8及び13週に圧力トランスデューサーを用いて椎間板内圧最低値を測定した。
- 【結果】
- コンドリアーゼ投与群の投与後13週における椎間板内圧最低値は、コンドリアーゼ1U/disc群では投与前値の48.5%、50U/disc群では投与前値の24.5%に低下し、PBS群と比較し有意差が認められた。
11)より一部改変
(4)椎間板ヘルニア症状改善作用(イヌ)12)
椎間板ヘルニアに罹患したイヌの椎間板内にコンドリアーゼを単回投与することにより、椎間板ヘルニアの臨床症状の改善が認められた。
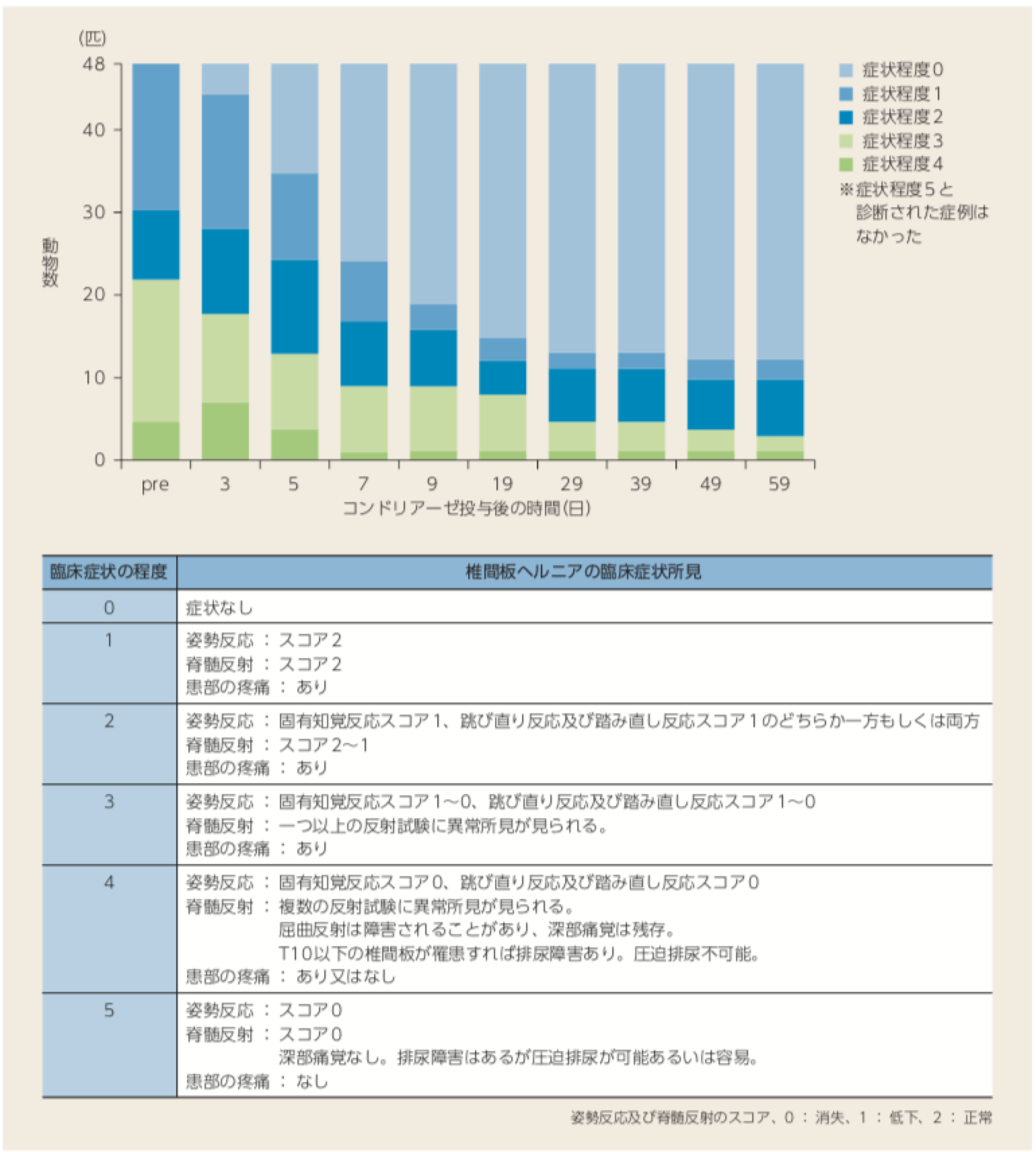
椎間板ヘルニア罹患イヌにおけるコンドリアーゼ投与後の臨床症状の変化
- 【方法】
- 椎間板ヘルニアの臨床症状を有する雌雄イヌ48匹の椎間板内に、250単位(U)/mLのコンドリアーゼを20~200μLの用量で単回投与した。コンドリアーゼ投与前から経時的にヘルニア臨床症状の程度を集計した。
- 【結果】
- コンドリアーゼ投与により椎間板ヘルニア症状の改善がみられ、投与後7日では24例(50%)の椎間板ヘルニアの臨床症状が消失した。
投与後9日以降も改善は緩やかに進行し、投与後59日では36例(75%)において椎間板ヘルニアの臨床症状が消失した。
12)より一部改変
臨床成績
国内第Ⅲ相プラセボ対照二重盲検群間比較試験〔承認時評価資料〕
臨床試験では「膨隆・突出型の腰椎椎間板ヘルニア」の症例も含まれていましたが、症例数が少なく検証が十分ではないことから、効能・効果は「保存療法で十分な改善が得られない後縦靱帯下脱出型の腰椎椎間板ヘルニア」となっています。一部承認された効能・効果とは異なるデータが含まれていますのでご留意ください。
- 試験デザイン
- 多施設共同、プラセボ対照、無作為化、二重盲検、群間比較
- 目的
- ヘルニコア(コンドリアーゼ1.25単位/mL)の有効性について、投与後13週における過去24時間の最悪時下肢痛(VAS)を主要評価とし、プラセボに対する優越性を検証する。また、投与後52週まで継続して安全性を評価する。
- 対象
- 腰椎椎間板ヘルニア患者
- 評価例数(FAS:Full analysis set、最大の解析対象集団)
- 163例(ヘルニコア群 82例、プラセボ群 81例)
- 試験方法
- ヘルニコア群とプラセボ群を1:1 に無作為に割り付けし椎間板内に単回投与した。投与後1 日までは入院期間とし、その後52 週まで外来で経過観察を行った。
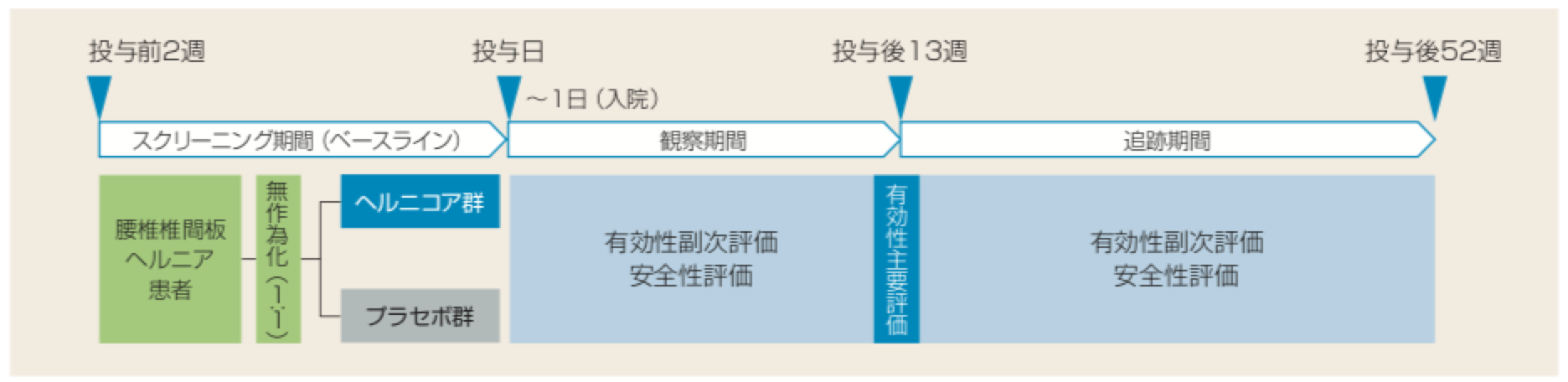
有効性(FAS)
- 主要評価項目
- 投与後13週における過去24時間の最悪時下肢痛(VAS)aのベースラインからの変化量
- a:ベースライン及び投与後13週のVAS値は連続する7日間の測定値の平均値
- 副次評価項目
- 投与後52週までの下記評価項目
過去24 時間の最悪時下肢痛(VAS)b の経時的推移、ODI の変化量、ヘルニア体積の変化量など - b:ベースライン、投与後1~6週及び13週のVAS値は連続する7日間の測定値の平均値
安全性(SAFETY:安全性に関する解析対象集団)
- 評価項目
- 有害事象、椎間板及び椎間板周辺組織の安定性(椎間板高、椎間の後方開大角度、椎体のすべり、軟骨終板と隣接する椎体の変化、椎間板の変性)、抗体検査など
(13週以降は下肢痛、腰痛、神経学的検査、椎間板及び椎間板周辺組織の安定性に関する有害事象のみ調査)
- 解析計画
- 主要評価項目は、ベースライン値及び下肢痛持続期間を共変量とした共分散分析を行い、欠測値はLOCF(Last observation carried forward)により補完する。
副次評価項目(追跡調査含む)は、共変量をベースライン値及び下肢痛持続期間とし、計量値の評価項目に対しては共分散分析、計数値の評価項目に対してはロジスティック回帰分析を行い、欠測値はLOCF により補完する。また、各時点のデータを要約し、推移を検討する。
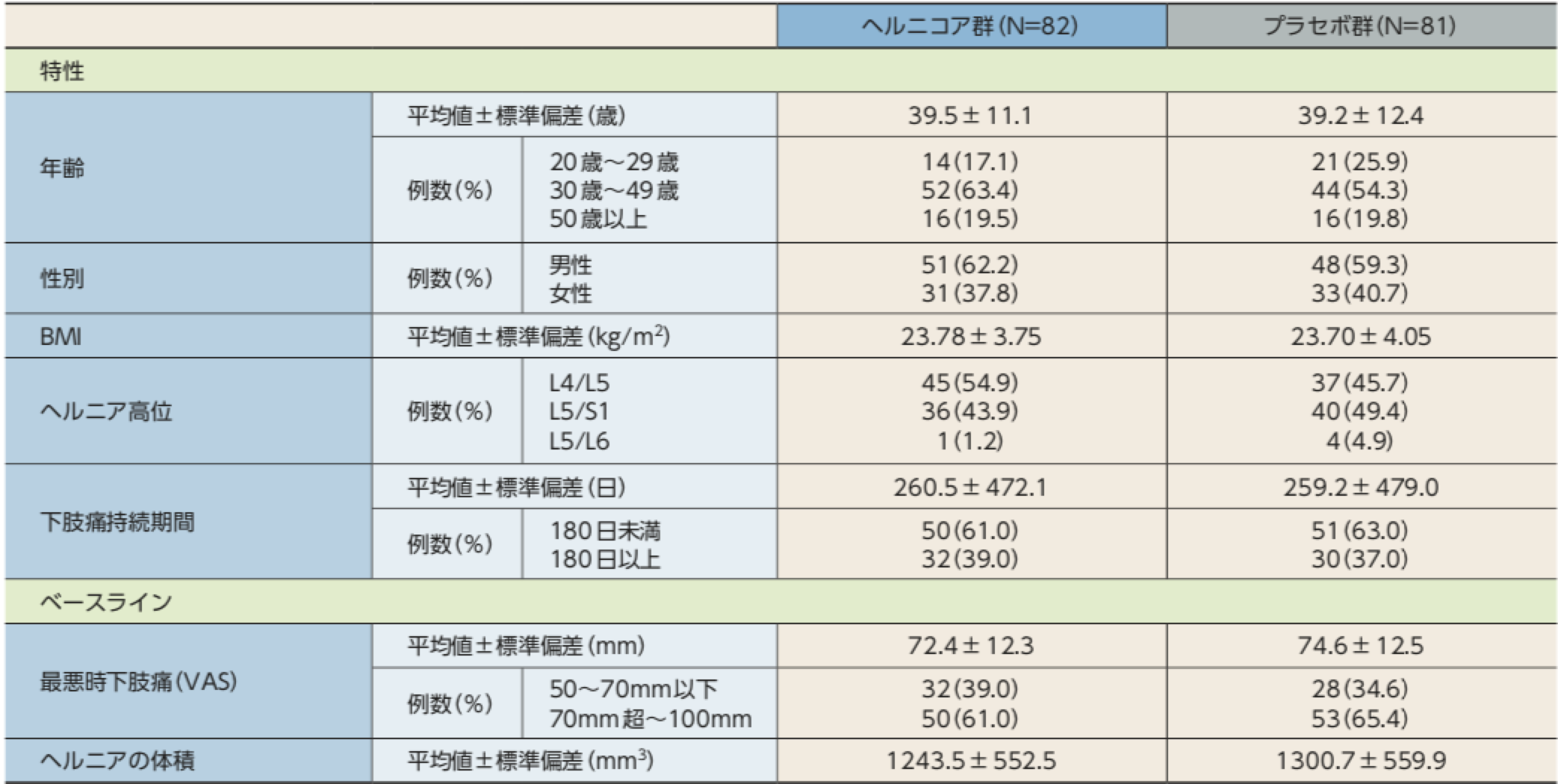
患者背景(FAS)
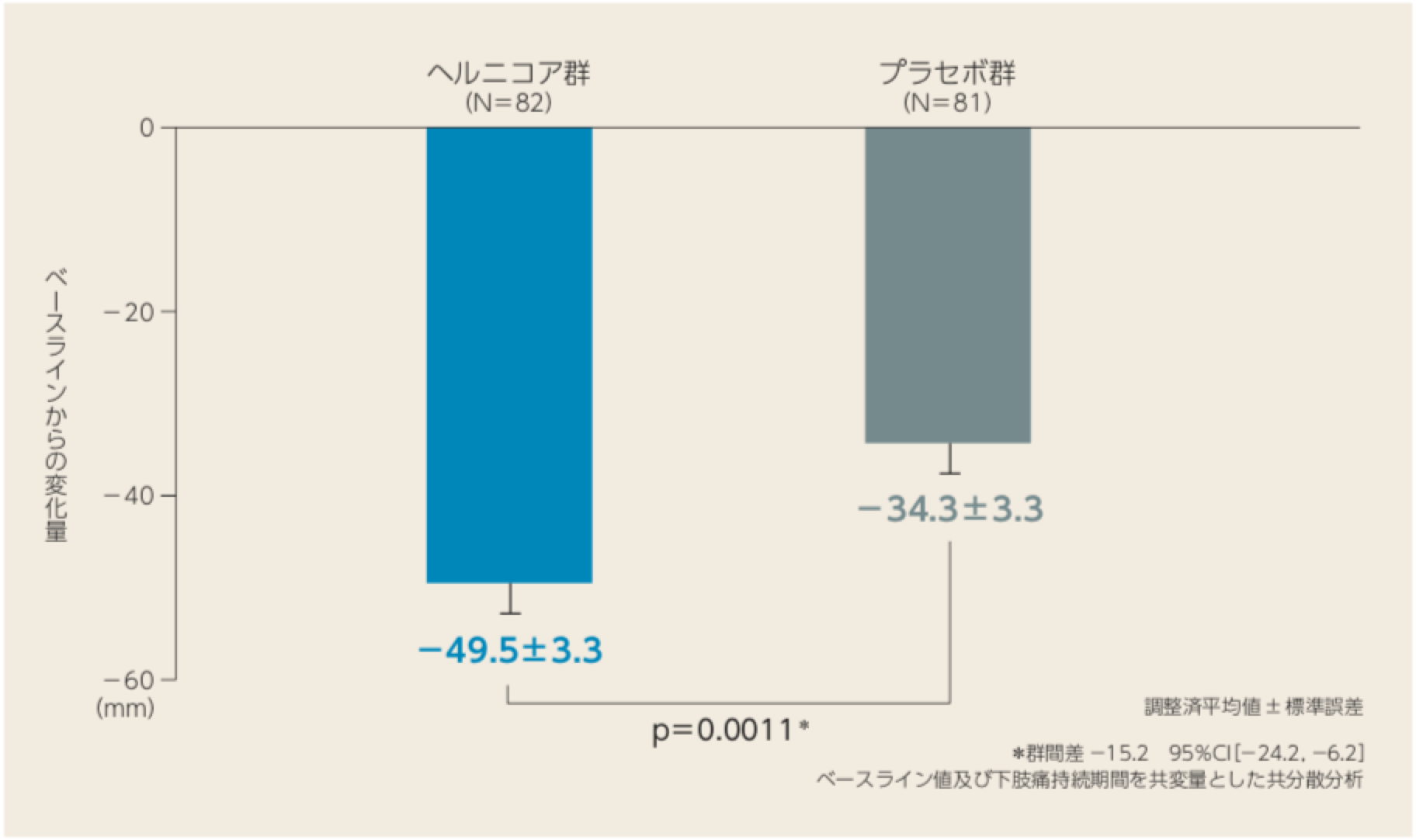
[主要評価項目]
投与後13週における最悪時下肢痛(VAS)の変化量
投与後13週の最悪時下肢痛(VAS)のベースラインからの変化量は、ヘルニコア群-49.5mm、プラセボ群-34.3mmであり、ヘルニコア群のプラセボ群に対する優越性が検証された(p=0.0011 共分散分析)。
投与後13週における最悪時下肢痛(VAS)の変化量(LOCF)
[副次評価項目]
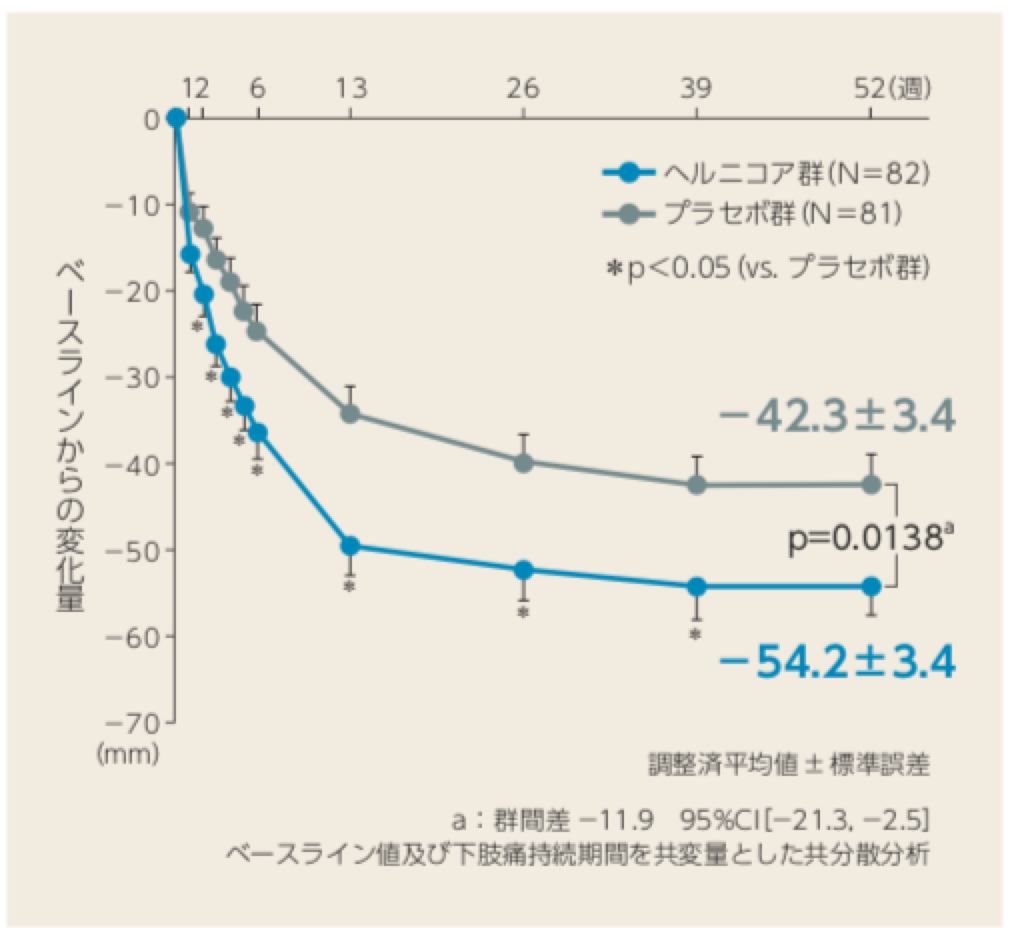
最悪時下肢痛(VAS)の経時的推移
最悪時下肢痛(VAS)のベースラインからの変化量は、投与後1 週より52 週まで経時的に低下した。
ヘルニコア群は投与後2 週から52 週までの観察時点において、プラセボ群との間に有意差が認められた。(投与後52 週時 p= 0.0138 共分散分析)。
最悪時下肢痛(VAS)の経時的推移(投与後52週まで)(LOCF)
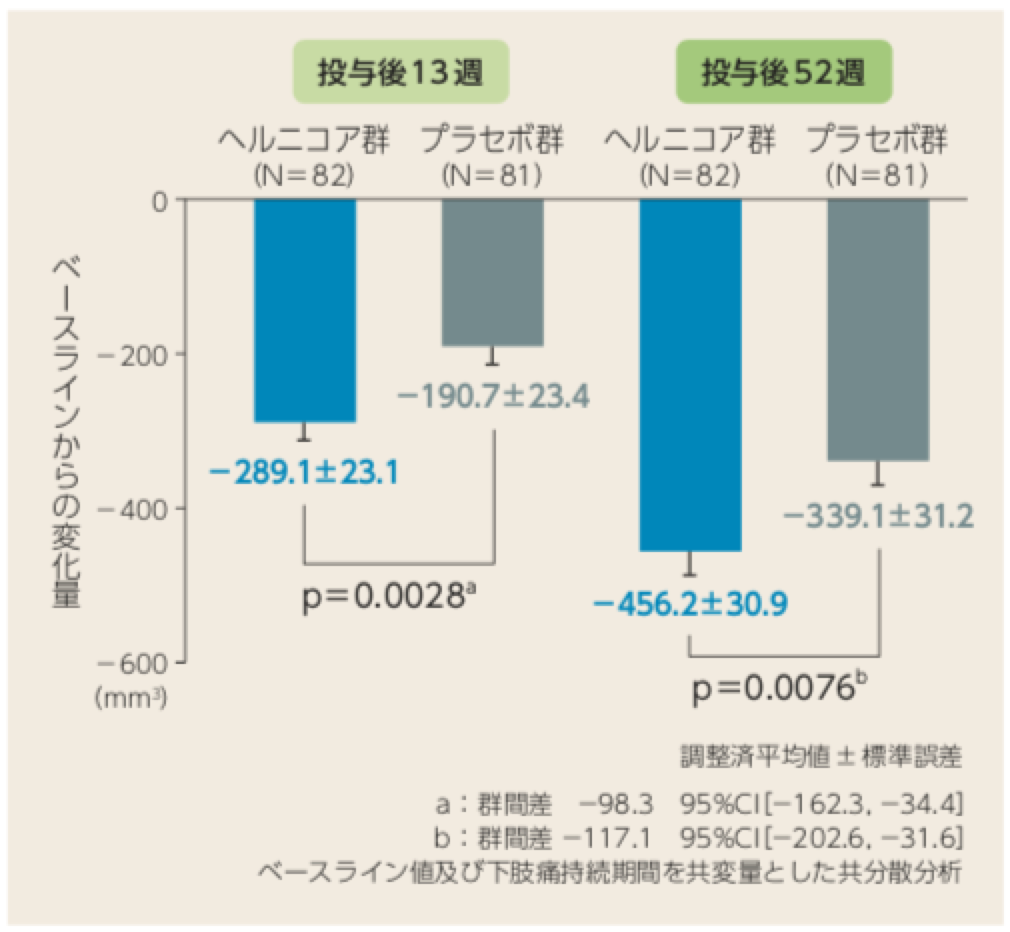
ヘルニア体積の変化量
投与後13週のヘルニア体積のベースラインからの変化量は、ヘルニコア群-289.1mm3、
プラセボ群-190.7mm3であり、プラセボ群と比較してヘルニコア群に有意な減少が認められた(p = 0.0028 共分散分析)。また、投与後52 週においても有意なヘルニア体積の減少が認められた(p = 0.0076 共分散分析)。
投与後13週、52週におけるヘルニア体積の変化量(LOCF)
[安全性]
副作用
副作用発現症例数は、ヘルニコア群82例中47例(57.3%)、プラセボ群81 例中27 例(33.3%)に認められた。ヘルニコア群で多く認められた副作用は、背部痛20例(24.4%)、核磁気共鳴画像異常20 例(24.4%)、脊椎X 線異常19 例(23.2%)であった。重篤な副作用は、ヘルニコア群の82例中1例(1.2%)に認められた背部痛であった。
重度の副作用はプラセボ群では認められず、ヘルニコア群の82例中1例(1.2%)に中毒性皮疹が認められた。
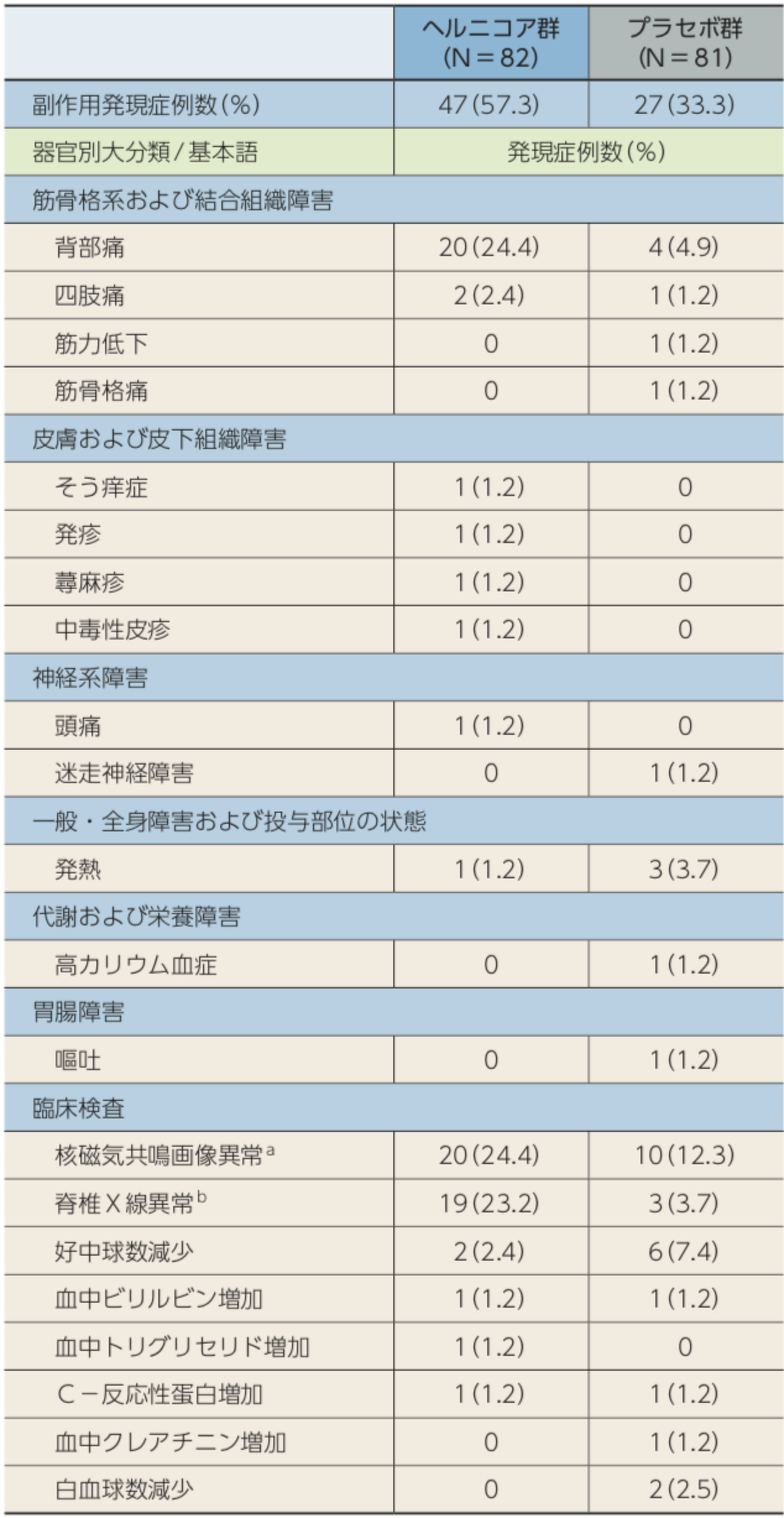
b: 30%以上の椎間板高低下、5°以上の椎間後方開大、3mm以上の椎体のすべり
MedDRA/J Ver.16.0
投与後52週までの全期間
椎間板及び椎間板周辺組織の安定性
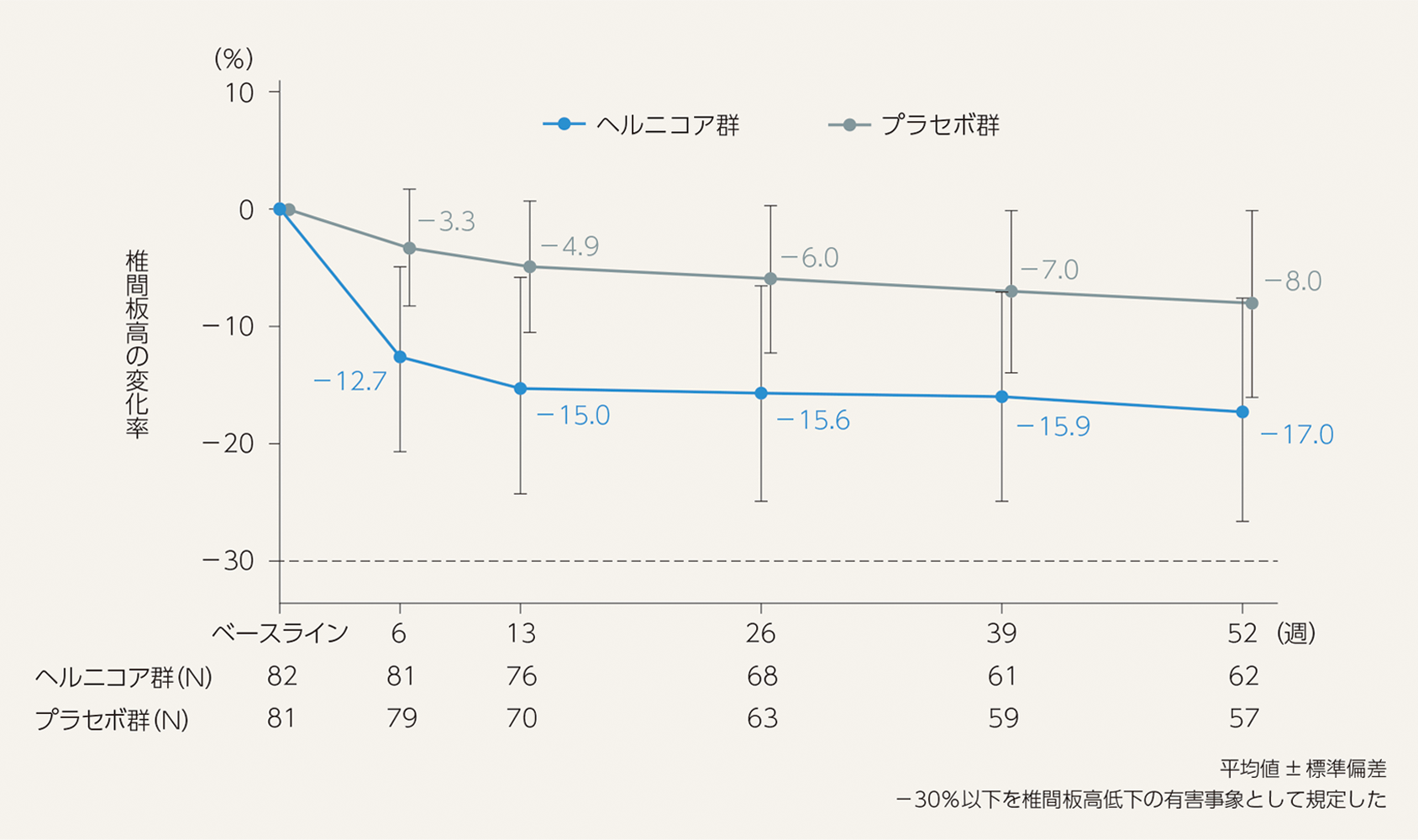
椎間板及び椎間板周辺組織の安定性として、「椎間板高の変化率の経時的推移」「椎間の後方開大角度の経時的推移」「椎体のすべりの経時的推移」を以下に示す。
椎間板⾼の変化率の経時的推移
椎間の後方開大角度の経時的推移
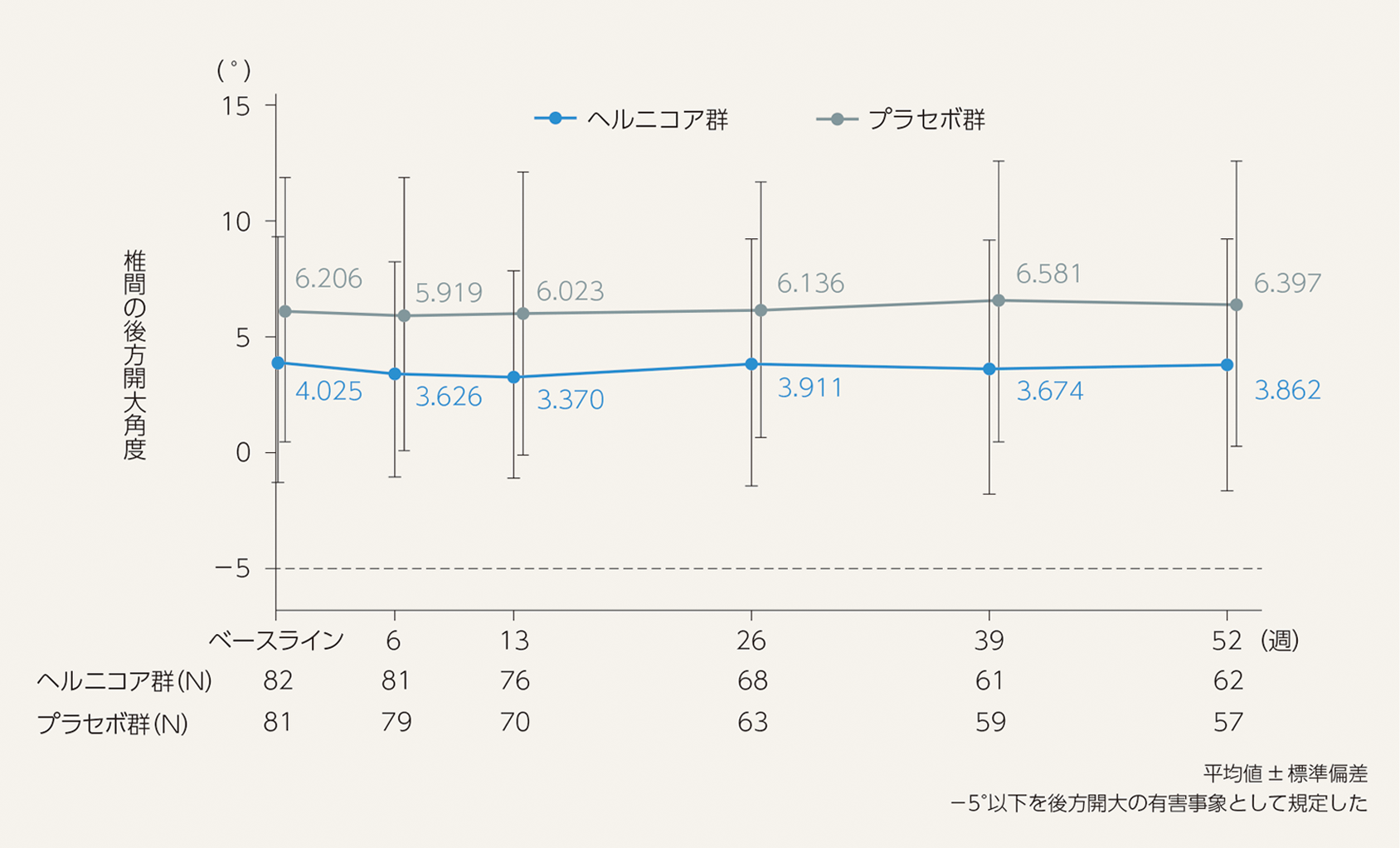
椎体のすべりの経時的推移
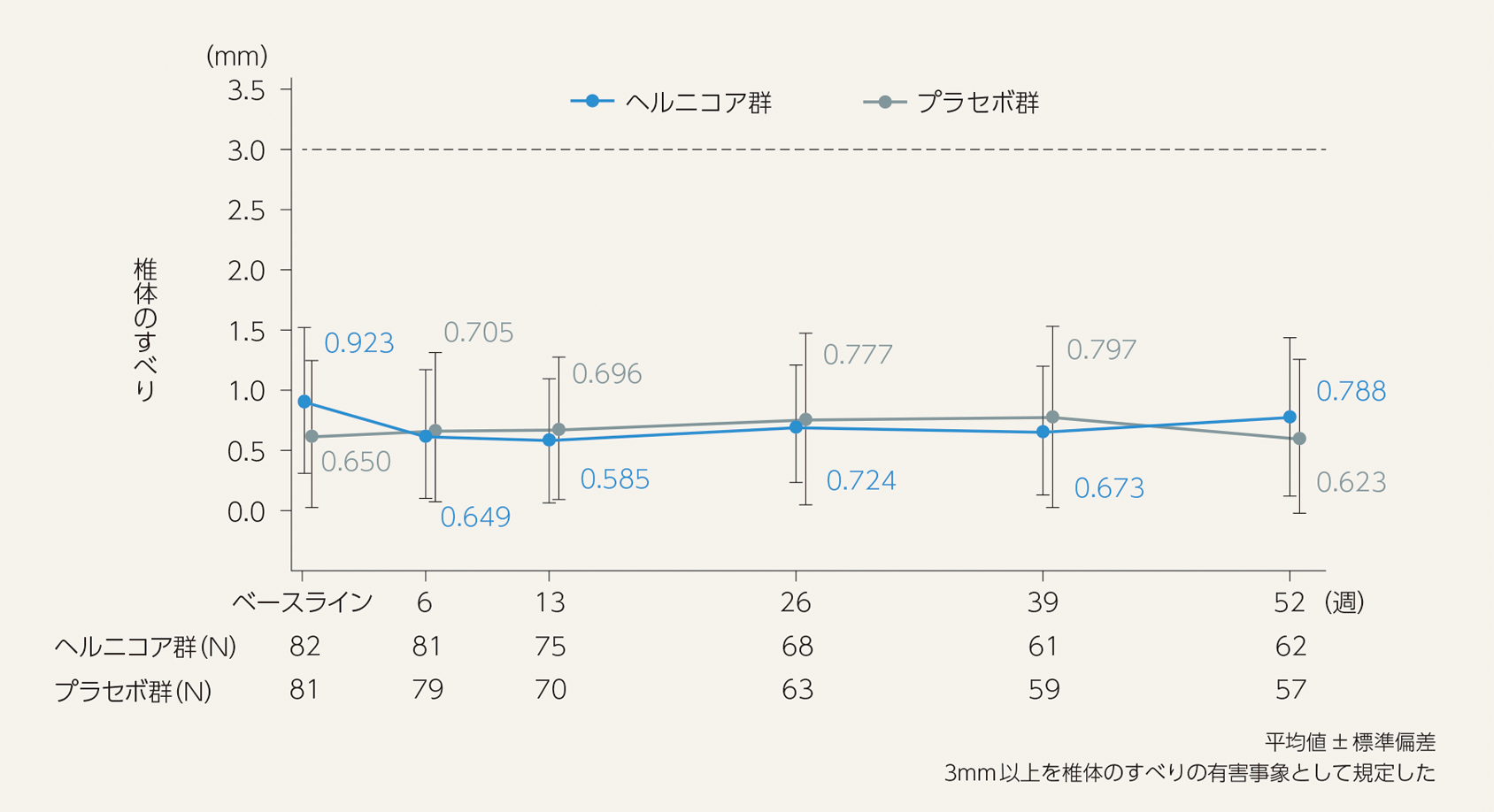
抗体検査
抗コンドリアーゼIgE 抗体価がベースラインと比較して上昇した症例は認められなかった。
抗コンドリアーゼIgG 抗体価がベースラインと比較して上昇した症例は、ヘルニコア群の1 例及びプラセボ群の2 例に認められた。
吸収試験の結果、ヘルニコア群の1例、プラセボ群の1例における抗体価上昇は、コンドリアーゼ特異的であることが確認されたが、抗体価上昇と関連が疑われるアレルギー様症状などの有害事象の発現は認められなかった。
生化学工業(株) 社内資料:腰椎椎間板ヘルニア患者を対象とした国内第Ⅲ相試験〔承認時評価資料〕より一部改変
主要文献
- 01)Fairbank JC, Couper J, Davies JB, O’Brien JP. The Oswestry Low Back Pain Disability Questionnaire. Physiotherapy. 1980; 66:271-273.
- 02)Fairbank JC, Pynsent PB. The Oswestry Disability Index. Spine 2000; 25:2940-2952.
- 03)生化学工業(株)社内資料:腰椎椎間板ヘルニア患者を対象とした国内第Ⅲ相試験(承認時評価資料)
- 04)福原 俊一 他 編著. SF-36 v2 日本語版マニュアル 健康関連QOL. 京都: 健康医療評価研究機構; 2004.
- 05)生化学工業(株)社内資料:腰椎椎間板ヘルニア患者を対象とした国内第Ⅱ/Ⅲ相試験(承認時評価資料)
- 06)生化学工業(株)社内資料:予後調査に関する臨床研究(承認時評価資料)
- 07)生化学工業(株)社内資料:国内臨床試験における薬物動態
- 08)生化学工業(株)社内資料:非臨床試験における薬物動態
- 09)生化学工業(株)社内資料:基質特異性試験
- 10)生化学工業(株)社内資料:正常ウサギを用いた薬理試験
- 11)生化学工業(株)社内資料:正常ヒツジを用いた薬理試験
- 12)生化学工業(株)社内資料:椎間板ヘルニア罹患イヌを用いた薬理試験
- 13)生化学工業(株)社内資料:安全性薬理試験
- 14)生化学工業(株)社内資料:カニクイザル単回椎間板内投与13週間病理観察試験
- 15)生化学工業(株)社内資料:カニクイザル単回椎間板内投与26週間観察試験
- 16)生化学工業(株)社内資料:ウサギ単回椎間板内投与試験
- 17)生化学工業(株)社内資料:イヌ単回椎間板内投与26週間観察試験
- 18)生化学工業(株)社内資料:イヌ単回椎間板内投与3年間観察試験
- 19)Bernick S, Cailliet R. Vertebral end-plate changes with aging of human vertebrae. Spine.1982;7:97-102.
- 20)Grignon B, Grignon Y, Mainard D, Braun M. Netter P, Roland J. The structure of the cartilaginousend-plates in elder people. Surg Radiol Anat. 2000; 22:13-19.
- 21)生化学工業(株)社内資料:マウス単回投与毒性試験
- 22)生化学工業(株)社内資料:ラット単回投与毒性試験
- 23)生化学工業(株)社内資料:イヌ単回投与毒性試験
- 24)生化学工業(株)社内資料:反復投与毒性試験(ラット、イヌ)
- 25)生化学工業(株)社内資料:生殖発生毒性試験
- 26)生化学工業(株)社内資料:遺伝毒性試験
- 27)生化学工業(株)社内資料:抗原性試験
- 28)生化学工業(株)社内資料:局所刺激性試験

